Leyes de los gases
¿Que son los gases?
se define a los gases como un estado de agregación de la materia en el que la misma no tiene una forma determinada debido a la dispersión y libre movilidad de las moléculas.Los gases tienen propiedades de expansión y compresión. Tipos de gas no afecta a razón de expansión o compresión. Todos los gases de expansión tiene misma constante.
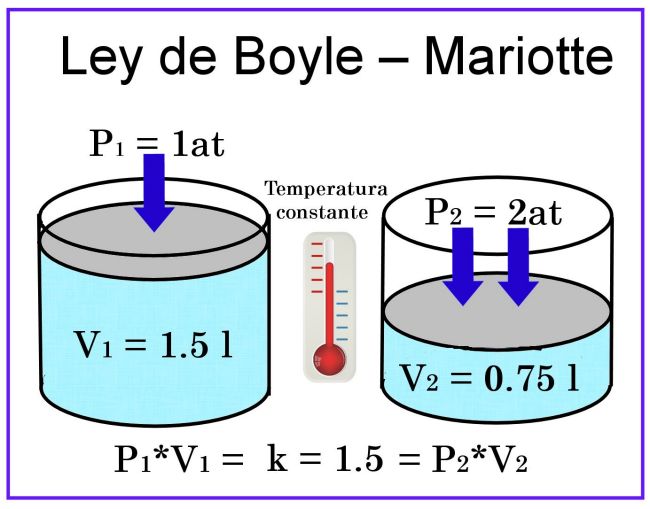
V es inversamente proporcional a P o
P.V=constante
Por otra parte;
P1.V1=P2.V2=P3.V3=.. (para el mismo gas a temperatura constante y el número de partículas.)
- Ejemplo: Gas con 150 cm3 de volumen tiene la presión de 120 cmHg. Si se aumenta el volumen del recipiente de 300 cm3, encontrar la presión final del gas.
- Ejemplo: Gas a 127 °C ha ml de volumen 240 ml. Si aumentamos la temperatura de gas de 127°C a 227 °C , encontrar el volumen final del gas.
T1=127+273=400 K
T2=227+273=500 K
V1=240 ml
V2=?
Usamos la ley de Charles para resolver este problema.
V1/T1=V2/T2
240/400=V2/500
V2=300 ml
3. / Gay Lussac Amonton la Ley: (relación presión-temperatura)
Cuando aumentamos la temperatura del gas, colocado en un recipiente con volumen constante, la velocidad del gas aumentan las moléculas. el aumento de la temperatura del gas a volumen constante y el número de partículas, aumentar la presión del gas.
- Ejemplo: Si queremos disminuir la presión de gas, colocado en un recipiente con volumen constante, de 4P de P lo mucho que debe cambiar la temperatura de la misma. Su temperatura actual es de 127 °C.
P1=4P
P2=P
T1=127 0C=127+273=400 K
P1/T1=P2/T2
4P/400=P/T2
T2=100 K=t+273
t=-173 0C
4. Ley de Avogadro: (Volumen-Número de la relación de las partículas)
Gases, con la misma presión y temperatura, tienen el mismo número de partículas en la misma cantidad de volúmenes. En otras palabras, el volumen y número de partículas de los gases son directamente proporcionales entre sí. Nos dijo que en los temas anteriores de que el gas es 22,4 litros 1mol bajo estándar de presión y temperatura y el gas 1mol contiene 6,02 x1023 moléculas / átomos. Podemos resumir esta relación con la siguiente ecuación:
Ejemplo: si 5 g O2 gas tiene un volumen de 200 cm3, encontrar el volumen de 20 cm3 de O2 en las mismas condiciones. (O = 16)
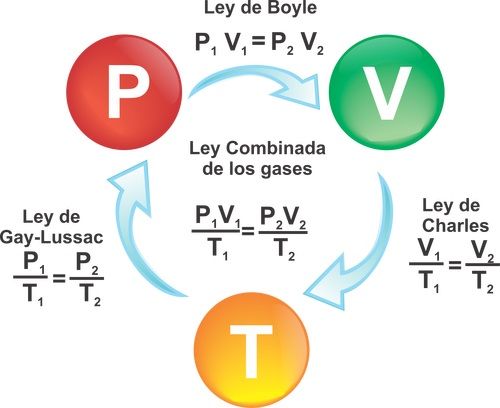
5.Ley del Gas Ideal La ley de los gases ideales
es la ecuación de estado del gas ideal, un gas hipotético formado por partìculas puntuales, sin atracción ni repulsión entre ellas y cuyos choques con perfectamente elàsticos. Se observan una serie de relaciones entre la temperatura, la presión y el volumen que dan lugar a la ley de los gases ideales.


Comentarios
Publicar un comentario